| Rev Esp Endocrinol Pediatr 2012;3 Suppl(1):198-209 | Doi. 10.3266/RevEspEndocrinolPediatr.pre2012.Apr.120 |
| Crecimiento |
| Sent for review: 18 Apr. 2012 | Accepted: 18 Apr. 2012 | Published: 30 Apr. 2012 |
| Congreso SEEP |
| Correspondence:Congreso SEEP |
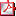 Tabla - P1d2d3-127 Tabla - P1d2d3-127 |
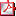 Tabla - P1d2d3-128 Tabla - P1d2d3-128 |
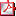 Tabla - P1d2d3-138 Tabla - P1d2d3-138 |
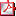 Tabla 1 - P1d2d3-136 Tabla 1 - P1d2d3-136 |
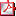 Tabla 1 - P1d2d3-137 Tabla 1 - P1d2d3-137 |
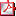 Tabla 1 - P1d2d3-142 Tabla 1 - P1d2d3-142 |
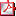 Tabla 2 - P1d2d3-137 Tabla 2 - P1d2d3-137 |
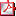 Tabla 2 - P1d2d3-142 Tabla 2 - P1d2d3-142 |
 Figura 1 - P1d2d3-131 Figura 1 - P1d2d3-131 |
 Figura 2 - P1d2d3-131 Figura 2 - P1d2d3-131 |
|
|
P1d2d3-127 SÍNDROME DE INSENSIBILIDAD A HORMONA DE CRECIMIENTO. NUEVA MUTACIÓN EN EL RECEPTOR DE HORMONA DE CRECIMIENTO. M.C. De Mingo Alemany, N. Pons Fernández, B Cremades Romero, E. Verdejo Gimenez, JA Cerón Pérez, F. Moreno Macián Hospital La Fe, Valencia INTRODUCCIÓN El Síndrome de Laron es una enfermedad extremadamente rara. Está causado por una anomalía en el gen que codifica el receptor de la hormona de crecimiento (GHR) localizado en 5 p14-p12. Tiene una herencia autosómica recesiva, por alteraciones en homocigosis o heteroicigosis compuesta. Estos pacientes presentan un profundo déficit de estatura que oscila entre -4 y -11.5 DE por debajo de la media, así como determinadas anomalías fenotípicas y riesgo de hipoglucemia. CASO CLÍNICO Paciente de 1 año de origen marroquí remitido para valoración de talla. Talla siempre por debajo de P3 con aplanamiento de la curva desde los 9 meses. Antecedentes familiares de cosanguinidad. Talla diana 169cm. Exploración física: Peso 7.8 Kg (P 0.28, -2.77 DE), Talla 63.8 cm (P0, -5.9 DE), PC 46 (P5, -1.64 DE). Frente olímpica, raíz nasal hundida, pelo ralo. Micropene, testes en bolsas, bolsas hipoplásicas. RM hipotálamo-hipofisaria: Hipófisis de pequeño tamaño con adecuada diferenciación de neuro y adenohipófisis, tallo hipofisario centrado. Estudio genético: secuenciación del gen GHR. Se encuentra un cambio A>G en homocigosis en el codón 575 (exón 6) que da lugar al cambio aminoacídico p.Tyr192Cys. Actualmente el paciente tiene 2.4 años, talla 70 cm (P0, -7.04 DE), velocidad de crecimiento1.86 cm/año. Está pendiente de iniciar tratamiento con IGF1 recombinante humana. DISCUSIÓN Presentamos el caso de un paciente con Síndrome de Laron que presenta una mutación en homocigosis en el exón 6 del gen GHR no descrita previamente. Se han descrito más de 70 mutaciones desde deleciones a mutaciones puntuales (mutaciones sin sentido, de cambio de sentido, de empalme y dominantes negativas). La mayoría afectan al dominio extracelular del receptor (codificado en los exones 3-7). Algunos autores sugieren que pueda existir una correlación genotipo-fenotipo que permita explicar el amplio espectro clínico de estos pacientes. La mayoría de mutaciones en homocigosis ocasionan deficiencia extrema de IGF1.
P1d2d3-128 ¿QUÉ HAY DETRÁS DE UNA SOSPECHA CLÍNICA DE GH BIOLÓGICAMENTE INACTIVA? A.Eguireun Rodriguez (1), G.Grau (1), A. Vela (1), A. Rodriguez (2), I. Rica( 1) (1) Hospital Universitario de Cruces, (2) Hospital de Mendaro. Bizcaia La GH biológicamente inactiva (GHBI) es la última indicación de tratamiento con GH incluida en nuestra comunidad, en base a estos criterios: Talla<-2SDS y/o 2SDS inferior a talla diana; VC Objetivos: Analizar las características clínico-analíticas de pacientes controlados en un hospital terciario en los que clínicamente se sospechó una GHBI, desde el año 2008. Describir la proporción final de diagnósticos positivos y la evolución posterior de los pacientes. Pacientes y metodología: Hemos sospechado el diagnóstico en 24 pacientes [33,3% niñas; 95% prepuberales; antropometría neonatal normal; talla diana-SDS media:-1±0,8 (4 pacientes con TBF)]. Variables estudiadas: VC-SDS; Talla-SDS, Peso-SDS; Diferencia entre Edad cronológica y EO (EC-EO); IGF1-SDS para edad e IGFBP-3 (IMMULITE). Metodología del test de generación: extracción de IGF1 basal y tras 5 días de tratamiento con GH (dosis: 0.035 mg/kg/día). Con los resultados del test y la evolución posterior de los pacientes hemos establecido 3 subgrupos: patología no confirmada, GHBI y déficit de IGF-1. Soporte estadístico SPSS18. Resultados: Diagnósticos: GHBI en 13 pacientes /déficit de IGF1 en 2 pacientes/ no patología demostrada en 9 pacientes (4 tuvieron IGF1 basal normal en día del test y 5 normalizaron espontáneamente la VC e IGF1). Del subgrupo con GHBI, 5 pacientes llevan 1 año en tratamiento con GH. La proporción de IGF1< -2 SDS es mayor en el subgrupo con diagnóstico de GHBI (61,5% vs 11,1%; Test exacto de Fisher, p= 0,031). El valor medio de IGF-BP3 fue inferior en este subgrupo (2,6±0,7 vs 3,6±0,88; U-Mann Whitney, p=0,029). No hemos encontrado otras diferencias (% de IGF1< -1SDS, edad cronológica ó datos clínicos previos) que permitan diferenciar ambos subgrupos. Conclusiones: El diagnóstico de GHBI se ha mantenido solo en la mitad de los casos en los que hubo una sospecha durante el seguimiento. En un contexto clínico compatible, un nivel de IGF1< -2 SDS con un valor disminuido de IGF-BP3, parecen los criterios analíticos que con mayor frecuencia se relacionan con esta entidad clínica.
P1d2d3-129 HEPATOPATÍA Y DÉFICIT DE HORMONAS HIPOFISARIAS. J. Cruz Rojo, J. Sánchez del Pozo, L. Garzón Lorenzo, M.T. Santos-García Cuellar, Á. Pérez Díaz, M.E. Gallego Gómez Endocrinología Pediátrica, Hospital 12 de Octubre, Madrid. Presentamos el caso de una adolescente de 16 años y 7 meses diagnosticada e intervenida a los 2 años y 6 meses de un craneofaringioma supraselar. Como secuelas de dicha intervención, la niña presenta los siguientes déficits hormonales: 1) Déficit de GH: diagnosticado por valores de IGF1 y BP3 persistentemente disminuidos desde la cirugía y por GH tras estímulo inferior a 0,05 ng/ml. A pesar de esto, ha mantenido buena velocidad de crecimiento y ha alcanzado una talla final igual a la diana.; 2) Déficit de TSH tratado desde el postoperatorio inmediato (dosis actual 200 mcg/día); 3) Déficit de ADH; 4) Déficit de FSH/LH: tratado inicialmente con valerato de estradiol, y en la actualidad con parches dérmicos de estrógenos y progesterona vaginal. Asociado a los déficits hormonales presenta hepatopatía diagnosticada a los 4 años y 2 meses, a raíz de hipertransaminasemia. Actualmente está en fase de cirrosis con hipertensión portal y RMN-Abdominal compatible con esteatosis severa. La biopsia hepática muestra hepatopatía crónica con septos completos y esteatosis masiva (80%) con mínima esteatohepatitis asociada. Asocia también obesidad leve-moderada, hiperuricemia e hiperinsulinismo (glucemias normales en SOG). Como tratamiento de la esteatosis recibe metformina y suplementos de vitamina E. En resumen se trata de una adolescente con un déficit de GH de 14 años de evolución no sustituido, que ha desarrollado una cirrosis hepática con muy mala respuesta a las medidas farmacológicas y de estilo de vida instauradas (dieta, ejercicio, metformina, vitamina E). Creemos que en la patogenia de dicha hepatopatía ha influido de forma muy significativa el déficit de GH (y consecuentemente de IGF-1 y BP3) de más de una década de duración. Actualmente, se ha iniciado tratamiento con GH mediante uso compasivo, dado que existen casos descritos en la literatura de mejoría de la esteatosis hepática en pacientes con déficit de GH tras la sustitución de dicha hormona.
P1d2d3-130 CONTROL EVOLUTIVO EN C.I.R. TRATADOS CON rHGH EN LOS ÚLTIMOS 5 AÑOS. M.C. Ontoria Betancort, M. López García, J.L. Castellano Pérez, M.I. García Camiñas, J.P. González Díaz Complejo Hospitalario Universitario de Canarias INTRODUCCIÓN: El objetivo del tratamiento con rHGH en los niños con talla baja, nacidos PEG y sin recuperación del crecimiento, es restaurar el mismo lo más próximo a la población de referencia o lo más cercano a la zona diana (parental). MATERIAL Y MÉTODOS: Estudio descriptivo retrospectivo de pacientes en tratamiento con rHGH diagnosticados de C.I.R. sin recuperación de la talla a los 4 años de edad, en los últimos 5 años. El análisis estadístico se realizó con el programa SPSS 17.0. RESULTADOS: Desde octubre de 2007 a enero de 2012 se siguió evolutivamente 33 pacientes, que representa el 42% del total de pacientes tratados con rHGH en nuestro Servicio durante dicho período. El 71,9 % eran mujeres y el 28,1 % varones. Edad gestacional: 31-41 semanas. Peso al nacimiento: -2,3 ± 1 DE. Longitud al nacimiento: -2,7 ± 0,8 DE. I. Al inicio del tratamiento: Edad: 6,2 ± 2,2 años. Talla: -3,15 ± 0,6 DE. Edad ósea: 1,3 ± 1 año inferior a la edad cronológica. Diferencia talla diana – talla inicial: 2 ± 0,8 DE. Talla media parental: 160,7 ± 7,5 cm. II. Evolución (tiempo de tratamiento: 6 meses - 4 años): talla evolutiva -2,01 ± 1,16 DE. Incremento de talla (talla evolutiva – talla inicial) 1 ± 0,6 DE (p< 0,001). Aproximación de la talla evolutiva a la talla diana 0,7 ± 1,4 DE (p<0,001). Dosis de tratamiento: 30 – 50 mcg/Kg/día. No se observó ninguna incidencia reseñable durante el tratamiento. CONCLUSIONES: Las diferentes variables analizadas en este estudio relacionadas con el crecimiento en pacientes C.I.R. tratados con rHGH alcanza los objetivos propuestos al inicio del tratamiento: 1. Ritmo de crecimiento: recuperación de la talla, aproximación a la talla diana, talla en rango poblacional (> P 3). 2. Optimizar la dosis de tratamiento (30-50 mcgr/Kg/día). 3. No efectos adversos clínico-analíticos.
P1d2d3-131 EL TRATAMIENTO CON HORMONA DE CRECIMIENTO (GH) DURANTE TRES AÑOS EN NIÑOS NACIDOS PEQUEÑOS PARA SU EDAD GESTACIONAL (PEG) MEJORA LOS COCIENTES DE RIESGO ATEROGÉNICO. M. Güemes Hidalgo (1), N. Fernández de Larrea Baz (2), C. Villalba Castaño (1), M. T. Muñoz Calvo (1), J. Argente Oliver (1) (1) Unidad de Crecimiento y Metabolismo, Hospital Infantil Universitario Niño Jesús, Madrid. (2) Agencia Laín Entralgo, Consejería de Salud de La Comunidad de Madrid Introducción: Diversos estudios han demostrado la asociación entre niños PEG y disminución de la sensibilidad a la insulina, e incluso el desarrollo de DM tipo 2, dislipemia y otros factores de riesgo cardiovascular en la edad adulta. Objetivo: Analizar la seguridad del tratamiento con GH durante 3 años en niños PEG seguidos a lo largo del período comprendido entre 2003 y 2011, determinando su influencia sobre la maduración ósea, el metabolismo de los carbohidratos, los lípidos, el perfil tiroideo y la tensión arterial. Metodología: Se estudiaron retrospectivamente los datos analíticos de 52 pacientes PEG (29 niñas y 23 niños) tratados con GH (dosis media: 0,035 mg/Kg/día, vía subcutánea), evaluándose los siguientes parámetros: edad ósea (Greulich & Pyle), glucemia, insulinemia, índice HOMA, hemoglobina glicosilada (HbA1c), perfil lipídico, T4L y tensión arterial. Resultados: La edad media de la cohorte estudiada fue de 5,9±2 años, con unos parámetros analíticos y tensionales pretratamiento dentro de la normalidad. El tratamiento con GH determinó un incremento significativo de la velocidad de crecimiento (p<0,001), junto con una aceleración significativa de la maduración ósea (p<0,001), permaneciendo dentro de los límites de la normalidad. Ello se acompañó de un aumento progresivo de los niveles de glucemia en ayunas, HbA1c (p<0,05 en ambos), insulina basal e índice HOMA (p<0,001 en ambos) (figura 1). Por el contrario, no se objetivaron cambios significativos en los niveles de colesterol total, triglicéridos, T4L ni en la tensión arterial. Sí se constató un cambio significativo en el descenso de C-LDL (p<0,05) y en el aumento de C-HDL (figura 2). Asimismo, los cocientes colesterol total/C-HDL y C-LDL/C-CHDL descendieron de forma significativa (p<0,05 y p<0,001, respectivamente). Conclusión: El tratamiento con GH, además de promover el crecimiento físico en pacientes PEG, genera una cierta resistencia a la acción de la insulina, y una mejoría de los cocientes de riesgo aterogénico a lo largo del seguimiento tras tres años de terapia. Estos hechos requieren una especial valoración en la pubertad y cuando el paciente alcance su talla adulta.
P1d2d3-132 EVOLUCIÓN DE UNA COHORTE DE NIÑOS PEQUEÑOS PARA SU EDAD GESTACIONAL TRATADOS CON HORMONA DE CRECIMIENTO. ANÁLISIS A UN AÑO DE EFECTIVIDAD Y SEGURIDAD J.P. López Siguero (1), M.J. Martinez-Aedo (1), J.A. Bermudez (2), N. Cabrinety (3), J.L. Lechuga (4) , J. Bosch (5), R. Espino (6), A. Gutierrez (7), F. Macías (8), M. Nuñez (9), B. De Gregorio (10) y Grupo colaborativo (1) Materno-Infantil, Málaga. (2) Macarena, Sevilla. (3) Sagrado Corazón, Barcelona. (4) Puerta del Mar, Cádiz. (5) Arrixaca, Murcia. (6) Jerez, Cádiz; (7) Badajoz. (8) Arnau de Vilanova. (9) Valme, Sevilla. (10) Ntra Sra de Meritxell, Andorra Se presentan los resultados de eficacia y seguridad de un análisis intermedio (primer año) del estudio observacional multicéntrico (SGA 27143) sobre una cohorte de niños pequeños para su edad gestacional (PEG) tratados con GH. Objetivos 1.- Estudiar cambios en la sensibilidad insulínica que pudieran aumentar el riesgo de diabetes tipo 2, así como otros factores de síndrome metabólico. 2.- Describir cambios auxológicos tras el tratamiento con GH. Metodología Estudio observacional, no aleatorizado, de un solo brazo, abierto y ambispectivo de una cohorte de sujetos PEG tratados con GH de acuerdo a los criterios de inclusión del Ministerio de Sanidad. Sujetos: Cohorte de 230, de los que 206 fueron evaluables: todos ellos para análisis de seguridad (al menos tratados con una inyección) y 92 (55,4% varones) para análisis completo (cumplido un año de tratamiento). Variables: Datos demográficos: Edad, sexo, PRN, LRN, EG, Talla diana. Auxológicas: Talla, Velocidad de crecimiento, Peso, Estadio puberal, Edad ósea, Perímetro de la cintura (PC) y Tensión arterial (TA). Bioquímicos: Generales, lípidos, insulina, T4 libre, IGF-I, HOMA-IR. Efectos adversos. Análisis estadístico: descriptivo con datos expresados como medias, DS y SDS. Comparación de medias. Resultados Inicio de terapia a los 7,3 (2,65) años con talla de -2,97 sds. EG: 37,5(3,3) semanas, PRN: 2140 g .LRN: 43,15 cm (4,01). La altura aumentó de -2,97 a -2,25 sds (ganancia 0,72). VC: 8,7 cm al año (2,96 sds). El cociente EO/EC aumentó de 0,70 (0,18) a 0,78 (0.16). No modificaciones para el Peso, Estadio puberal (95% en estadio I basal y 90,6% al año), PC y TA. El HOMA-IR se incremento desde 1,34 (1,12) a 1,90 (1,76), con ganancia de 0,56 (1,49). No hubo modificaciones del resto de los parámetros metabólicos. Efectos adversos: 4 sujetos. Tiroiditis (1), Ansiedad (1), Picor en zona de inyección (1) e Hipertransaminasemia (retirada la GH). Conclusiones 1.- La GH estimula el crecimiento en niños PEG sin avance relevante de la edad ósea. 2.- El tratamiento muestra un buen perfil de seguridad, salvo por el aumento del HOMA-IR, que precisa un seguimiento a largo plazo.
P1d2d3-133 ANÁLISIS DEL TRATAMIENTO CON HORMONA DE CRECIMIENTO (GH) BIOSIMILAR EN NIÑOS PEQUEÑOS PARA EDAD GESTACIONAL M.J. Alcázar Villar, M. J. Rivero Martín, C. Navarro Moreno, M. Sanz Fernández Hospital Universitario de Fuenlabrada, Madrid INTRODUCCIÓN: En 2003 la Agencia Europea para la Evaluación de Medicamentos (EMEA) aprobó el tratamiento con GH para niños pequeños para edad gestacional (PEG) no sindrómicos, que a los 4 años presentan una talla por debajo de 2.5 DS (más de 1DS por debajo de la talla media parental) y sin crecimiento recuperador (velocidad de crecimiento menor de 0.5 DS). La dosis recomendada es de 0.035 mg/kg/día. OBJETIVO: analizar los resultados del tratamiento con GH biosimilar en nuestra población de niños PEG. MATERIAL Y MÉTODOS: Analizamos en 12 pacientes: sexo, tipo de gestación (única o múltiple), edad gestacional (EG), peso y talla al nacimiento (PRN,TRN), edad de inicio del tratamiento, dosis administrada, velocidad de crecimiento (VC) antes, al año y a los 2 años de tratamiento, edad ósea, y efectos secundarios. RESULTADOS: Proporción varones/niñas 1:2. El 33% de los niños procedían de embarazos gemelares, siendo el otro gemelo de talla normal. Mediana EG: 37 semanas (C1:35, C3:39) Media de PRN: -2,02 DE (DE:0,56), Media de TRN: -3,11 DE (DE:1.6).Edad media de comienzo de tratamiento: 5.69 años (DE 2.09). Dosis media de inicio: 0,032 mg/kg/día (DE:0,0035). VC previa al tratamiento: 6,02 cm (DE: 1.11) VC al año: 8.6 cm (DE 1.19)(P 98.5 DE:3.27).VC a los 2 años: 7.78 (DE 0.2).El 84% de los pacientes llevaba un año de tratamiento y el 16% dos. Ganancia de talla media al año: 0,7 DE (DE: 1.17).Sólo se encontró la edad ósea retrasada en uno de los pacientes. Efectos secundarios: uno de los pacientes precisó sustitución del biosimilar por otra presentación con dispositivo de aguja oculta por fobia a las agujas. El 18% (2) de los pacientes presentaros efectos secundario que consideramos leves: uno hipotiroidismo y otro hipercolesterolemia leve. Un paciente presentó aumento de la hipermetropía y en otro el aumento de IGF1 durante el tratamiento obligó a disminuir la dosis de GH. COMENTARIOS: Aunque la muestra analizada es de pequeño tamaño se observa recuperación de talla el primer año de tratamiento. La dosis media al inicio del tratamiento fue menor de lo recomendado, con media de VC el primer año en P98,5 (DE: 3,27).
P1d2d3-134 ESTUDIO RETROSPECTIVO DE UNA COHORTE DE PACIENTES EN EDAD PEDIÁTRICA TRATADOS CON GH. ANÁLISIS DE FACTORES RELACIONADOS CON LA RESPUESTA AL TRATAMIENTO. R. Monné Gelohch, M. Olona Cabaces, M. Escolà Llop Hospital Universitari Joan XXIII, Tarragona Objetivo: Describir las características de una muestra de 64 pacientes que han recibido tratamiento con hormona de crecimiento (GH) y analizar las variables que podrían influir en la respuesta al tratamiento. Métodos: Estudio observacional de tipo retrospectivo de los pacientes tratados con GH en el Servicio de pediatría del Hospital durante los últimos 14 años y que cumplen criterios de tratamiento con GH según el Comité Asesor de GH. Se analizan los siguientes parámetros: prematuridad, pequeño para la edad gestacional(PEG), talla baja familiar, alteración de la resonancia nuclear magnética (RNM), alteración genética, retraso en la edad ósea, pico de GH a un estímulo, niveles basales de IGF-1 y la edad al inicio del tratamiento. Estudio de los pacientes que han finalizado el tratamiento. Consideramos que hay respuesta al tratamiento si la talla final es ≥ -2 SD o ≥ a su talla diana. Se analizan las diferencias entre la cohorte que ha respondido al tratamiento y la que no. Análisis estadístico: para la comparación de grupos se ha utilizado la prueba de la Ji al cuadrado para variables categóricas y la U de Mann Whitney para variables continuas. El nivel de significación aceptado p≤0,05. Resultados: De los 64 pacientes estudiados 46 (71,9%) son de sexo masculino, 25 (31,9%) tienen antecedente de PEG y 16 (25%) de talla baja familiar. Un 21,8% de pacientes tiene RNM patológica; de estos un 42,8% tienen IGF 1 bajo respecto un 23,7% en los que tienen RNM normal, aunque la diferencia no es significativa. De los pacientes revisados, 19 (31,6%) han finalizado su crecimiento. En 12 (63,1%) se ha objetivado respuesta al tratamiento. Se ha hallado asociación entre la edad de inicio y la respuesta al tratamiento (11,1±3 vs 14,1±2; p=0,02). Conclusiones: El porcentaje de niños tratados con GH es mayor que el de niñas. Es frecuente que los niños tratados con GH tengan antecedente de talla baja familiar y/o PEG. La RNM patológica se asocia a bajos niveles de IGF1. De los factores analizados que pueden influir en la respuesta al tratamiento, el único que ha resultado significativo es el inicio precoz.
P1d2d3-135 UNA CAUSA DE TALLA BAJA DE INICIO PRENATAL S. Ortigosa Gómez, V. Seidel Padilla, G. Aznar Lain, M.A. López Vilchez, M. Bonet Alcaina Hospital del Mar, Parc de Salut Mar. Barcelona Introducción El crecimiento intrauterino restringido (CIR) incluye diversas causas que pueden conllevar talla baja, algunas de ellas de origen genético. El síndrome de Silver-Russell (SSR) es de las más conocidas, pero existen causas más excepcionales que también requieren estudio genético. Caso clínico Niño de 3 años y 9 meses en seguimiento por CIR sin crecimiento recuperador. Antecedentes: Primera gestación controlada. Cesárea a las 33 semanas por CIR severo. PN 1.045 g (-3,31 DE), longitud 37 cm (-3,88 DE), PC 29 cm (-2 DE). Hipoglucemias primeras horas de vida. CIA tipo ostium secundum con cierre espontáneo a los 7 meses. Trastorno de aprendizaje. Talla media parental -0,7 DE. Exploración física: Peso 11 kg (-2,25DE), Talla 88 cm (-3,47DE), PC 47,8 cm (-2,4DE). Cara triangular, frente prominente, microretrognatia, filtro amplio, labio superior fino, punta de nariz bulbosa, orejas de implantación algo baja, clinodactilia bilateral Vº dedo, surco palmar transverso único derecho y testes en ascensor. Estudio básico de talla baja normal excepto IGF-I <25 ng/ml. Cariotipo: 46,XY. Edad ósea igual a edad cronológica. Ante la sospecha de SSR se realiza estudio genético descartándose las 2 causas moleculares más frecuentes: hipometilación en H19 (región 11p15.5) y disomía uniparental materna del cromosoma 7. Por lo que se prosigue realizando MLPA de microdeleciones y regiones subteloméricas resultando normales. Finalmente el array de SNP 6.0 muestra deleción de 3,68 Mbp en 10q 26.13-26.2. Se solicita tratamiento con rhGH por CIR sin crecimiento recuperador. La deleción subterminal en el brazo largo del cromosoma 10 presenta características clínicas que se solapan con el SSR: retraso de crecimiento pre y postnatal, cara triangular, frente prominente, labio superior fino y clinodactilia de Vºs dedos. Otros casos publicados, de mayor tamaño, presentan además microcefalia, problemas genito-urinarios, retraso psicomotor y problemas de comportamiento. Conclusiones - El diagnóstico etiológico de CIR es difícil debido a las múltiples causas que pueden producirlo. - Destacar la importancia de la valoración por parte de genética clínica de los CIR sin crecimiento recuperador para su mejor filiación. - El correcto diagnóstico etiológico del CIR permitirá valorar de manera más objetiva la respuesta al tratamiento con rhGH.
P1d2d3-136 ESTUDIO COMPARATIVO DE EFICACIA DE DOS TIPOS DE HORMONA DE CRECIMIENTO: BIOSINTÉTICA Y BIOSIMILAR I. López Martínez, I. Rincón Mantilla; A. Sangil González; C. Moreno Cantó; E.I. Caballero Fernández; A. Domínguez García; S. Quinteiro González Hospital Universitario Insular Materno-infantil, Gran Canaria El biosimilar de la hormona de crecimiento (GH) está comercializado en España desde 2007 y es escasa la literatura que lo compara con la hormona de crecimiento biosintética. Objetivo: Comparar la eficacia y seguridad de GH biosimilar (grupo A) y biosintética (grupo B) tras un año de tratamiento en un grupo de pacientes diagnosticados de déficit de GH. Metodología: Estudio observacional retrospectivo no aleatorizado que compara un grupo A (n=15) y un grupo B (n= 16), todos ellos diagnosticados de déficit aislado idiopático de GH demostrado con dos pruebas dinámicas (ejercicio y clonidina) con una respuesta menor de 10 ng/ml. Se han considerado como variables independientes: edad, sexo, talla, dosis de GH y edad ósea. Como variable dependiente: velocidad de crecimiento (VC) al año de tratamiento (EO). Los datos han sido analizados con t-student para muestras independientes o su equivalente no paramétrico de Mann-Whitney y test de independencia de chi-cuadrado. Nivel de significación: 0,05. Resultados: Edad de inicio del tratamiento: 10,02 (3.5) años en el grupo A y de 9.85 (3.36) años en el B con una talla media en SDS al inicio de -2,79 (0.89) para el grupo A y de -2.80 (0.8) para el B. La distribución por sexos fue semejante en ambos grupos. La dosis media en el grupo A fue de 32,49 (4,33) microgramos/K/día y para el B de 35 (4,33) microgramos. La edad ósea, talla diana, evolución de la talla, VC y la relación edad ósea-cronológica se exponen en la tabla 1. No se han observado efectos adversos en ninguno de los grupos. Conclusiones: No se han encontrado diferencias en cuanto a eficacia de acción y seguridad en ambos grupos.
P1d2d3-137 ESTUDIO DE PARÁMETROS DE RIESGO METABÓLICO EN PACIENTES CON RETRASO DEL CRECIMIENTO INTRAUTERINO Y SU RELACIÓN CON EL TRATAMIENTO CON HORMONA DE CRECIMIENTO A.Rodríguez Estevez (1), C. Fernandez Ramos (2), L. Martinez-Indart (3), I. Rios Orbañanos (1), B. Pacho del Castaño (1) y Grupo de Endocrinología Pediátrica de CAV: I. Rica Etxebarria(1), A. Vela de Sojo (1), G. Grau Bolado (1), FJ. Nuñez Rodríguez(2), I. Díez López (4); A. Sarasua Miranda (4); E. Artola Aizalde (5), V. Cancela Muñiz (5), E. Blarduni Cardón (6), A. Eguireun Rodríguez (7) (1) Endocrinología Pediátrica-Hospital Universitario de Cruces. Barakaldo, (2) Hospital Universitario de Basurto, Bilbao, (3) Unidad de Epidemiología Clínica, Hospital Universitario de Cruces, Barakaldo, (4) Hospital Universitario de Álava, Vitoria, (5) Hospital Universitario de Donosti, Donosti, (6) Hospital de Zumárraga, Zumárraga, (7) Hospital de Mendaro, Mendaro Objetivos: Analizar los parámetros de riesgo metabólico en la población con Retraso del Crecimiento Intrauterino (RCIU) al inicio y durante el tratamiento con hormona de crecimiento (GH) de nuestra Comunidad Autónoma. Pacientes y Metodología: Estudio retrospectivo de los pacientes RCIU de nuestra Comunidad en tratamiento con GH. Fuente: formularios del Comité Asesor del Servicio de Salud. Establecimos 2 grupos en función del HOMA-IR (£ o > 3.16). Se evaluaron otros parámetros de riesgo metabólico: HDL-C, Triglicéridos (TG), Tensión Arterial Sistólica (TAs) y Diastólica (TAd) y la dosis de GH. Las variables categóricas se han descrito mediante porcentajes y las variables continuas mediante medias y desviaciones típicas. La comparación de diferentes variables y el HOMA <3.16 y >3.16 se ha realizado mediante la prueba no paramétrica de U de Mann Whitney. Resultados: 76 pacientes (43 V, 45 M). Longitud nacimiento 42.9 ± 4.3 cm (-2.8±1.2) y Peso nacimiento 2067,9±680gr (-2.1±0.7DE). 31% eran pretérminos (<37 s). El grupo de pacientes con HOMA-IR > 3.16 se duplicó durante el tratamiento con GH (tabla 1). Los RCIU con HOMA-IR £3.16 tenían una media de IGF-1 menor (tabla 2) tanto al año como a los 4 años de tratamiento, siendo esta diferencia estadísticamente significativa; y era independiente del estadio puberal (prepúber/púber). A lo largo del seguimiento el porcentaje de RCIU que iniciaron pubertad fue aumentando: 5.7%, 14.8% y 58.8% al inicio, 1 año y 4 años de GH. No encontramos diferencias estadísticamente significativas entre el HOMA-IR al año y 4º año de tratamiento con el resto de parámetros estudiados Conclusiones: El grupo RCIU con HOMA-IR >3.16 se duplicó al año de tratamiento con GH, siendo este parámetro de riesgo metabólico el único que hemos encontrado alterado. Este grupo presentaba asimismo unos valores de IGF-1 superiores al grupo con HOMA-IR £3.16.
P1d2d3-138 CARACTERÍSTICAS DE LOS PACIENTES TRATADOS CON HORMONA DE CRECIMIENTO (GH) EL PERIODO 2008-2011 EN UN SERVICIO DE PEDIATRÍA DE RECIENTE CREACIÓN I. Mulero Collantes, E. Santamaría Marco,. J.C.Hernando Mayor Hospital Universitario Rio Hortega. Valladolid Introducción. Existen diversos datos sobre los efectos de la GH en diversas patologías y diferencias en los resultados obtenidos en la ganancia de talla. Objetivos. Conocer las características clínicas más relevantes y la respuesta al tratamiento con GH en nuestra serie de pacientes. Materiales y métodos. Se presentan 19 pacientes en tratamiento con rhGH iniciado durante este periodo y se valoran sus velocidades de crecimiento pre/post-tratamiento así como sus peculiaridades clínicas. Resultados. 1) Déficit clásico GH: 12 pacientes (8 niñas/4 niños), origen hindú y ruso de dos pacientes (adopción internacional). Hallazgos en RMN: hipoplasia hipofisaria (3 casos), un caso de neurohipófisis ectópica relacionado con alteración en la línea media (fisura palatina y labio leporino), y una aplasia hipofisaria con neurohipófisis ectópica en relación con un panhipopituitarismo. Un caso era además CIR (trillizo, PRN 1120gr, TRN 31,5cm, 34 SEG). Mejoría media de talla de +1,02 DS el primer año. 2) Síndrome de Turner (2 pacientes): Una de ellas asociaba H.pylori de difícil erradicación. La otra asociaba obesidad, insulinorresistencia, hipertransaminasemia y esteatosis hepática, con diagnóstico tardío (11 años) y origen dominicano. Mejoría de talla de +0,09 DS el primer año. 3) Alteraciones del gen SHOX (1 paciente): Fenotipo peculiar en madre y niño (síndrome de Leri-Weill). Anomalía de Madelung en Rx edad ósea. Mejoría de +1,58 DS al año. 4) CIR (3 casos): En RMN de uno de ellos, quiste aracnoideo en cisura coroidea derecha. Mejoría de talla de +0,52 DS el primer año. 5) TBI (1 caso): Mejoría de talla +0,66 DS al año de tratamiento. Conclusiones: Todos los casos del 1 al 4 cumplen criterios de tratamiento con GH indicados por el Comité Nacional/Autonómico según el momento. Importante señalar la limitación en la valoración de la población inmigrante y/o adoptada, debido a la utilización de gráficas españolas. Hallazgos patológicos en RMN en el 41% de los pacientes con déficit de GH de nuestra serie. Importancia de la exploración física (acortamiento rizomiélico de EESS en familiares, fenotipo Turner…) y de la patología asociada (alteraciones anatómicas, obesidad, resistencia insulínica…). La mejoría de talla tras el comienzo de la GH depende de muchos factores: diagnóstico inicial, edad de inicio del tratamiento, patología asociada, etc.
P1d2d3-139 GH BIOLÓGICAMENTE INACTIVA ASOCIADA A SÍNDROME DE NOONAN C. de Lamas Pérez (1), B. Huidobro Fernández (2), C. Quinteiro García (3), A.B. Martínez López (2), A. Rodríguez Sánchez (2); M.D. Rodríguez Arnao (2) (1) Hospital Clínico de Salamanca; (2) Hospital General Universitario Gregorio Marañón, Madrid (3) Unidade de medicina molecular - FPGMX, Complexo hospitalario universitario de Santiago de Compostela; Santiago de Compostela INTRODUCCIÓN: El síndrome de Noonan afecta a uno de cada 1000-2500 recién nacidos vivos; relacionado, aunque no siempre, con mutaciones en el gen PTPN11. Se caracteriza por la presencia de un fenotipo especial con hipogonadismo hipergonadotropo, malformaciones cardíacas, talla baja y afectación ósea. OBJETIVOS: Presentación de un caso de síndrome de Noonan en el que se asocia talla baja por GH y su evolución durante 5 años. CASO CLÍNICO: Niño de 3 años y 4 meses que acude para valoración de talla baja observada desde siempre, con disminución de la velocidad de crecimiento durante los últimos meses. Antecedentes personales y familiares: Embarazo controlado de curso normal; peso al nacimiento: 3400 g (+0DE); talla genética 181,5 cm (+0,65DE). Orquidopexia bilateral a los dos años. Exploración física: peso 14,2 Kg (-0,76DE), talla 90,5 cm (-2,29DE). Dismorfia facial con anteversión e implantación baja de los pabellones auriculares, eutiroideo. Genitales masculinos de configuración normal en estadío I de Tanner; con testes en bolsas de unos 2 ml de volumen. Hemograma, bioquímica y estudio tiroideo: normales. Estudio hormonal: TSH 2,57uUI/mL (rango de normalidad 0,5-4,5), T4 libre 1,3 ng/dL (0,6-1,4), cortisol 9,7 ug/dL (5-25), GH respuesta a clonidina: pico 11,7 ng/mL (>10), IGF1 <25,0 ng/mL (49-289), IGFBP3 0,8 ug/mL (0,9-4,3); test de generación de IGF1: IGF1 103 ng/mL, IGFBP3 3,0 ug/mL. RMN craneal: normal. Edad ósea: 3 años. Cariotipo: 46XY. Estudio molecular gen GH1: polimorfismo P1 en heterocigosis en el intrón IV; haplotipos H1/H11 en la región promotora proximal (madre H1/H14 y padre H11/desconocido), asociado el H11 con una disminución significativa (superior al 60%) en la expresión del gen. Estudio genético para síndrome de Noonan: mutación E76D (exón 3) en heterocigosis en gen PTPN11. Se inicia tratamiento con GH recombinante a los 4 años y 10 meses (0,28 mg/Kg/día). A los 8 años y 8 meses de vida: talla 132,5 cm (-0,13DE); peso 28,7 Kg (p30; -0,54DE); estadío I de Tanner. CONCLUSIONES: Ante la presencia de talla baja en un paciente es necesario descartar siempre que la existencia de cualquier causa para la misma susceptible de ser tratada.
P1d2d3-140 REVISIÓN AUXOLÓGICA TRAS FINALIZAR EL TRTATAMIENTO CON GH EN EL SÍNDROME DE TURNER O.M. López Moreira, J. González González, S. Bernal Cerrato, J.A. Bermúdez de La Vega Sección de Endocrinología de La UGC de Pediatría del Hospital Universitario Virgen Macarena, Sevilla INTRODUCCIÓN: El síndrome de Turner (ST) se caracteriza por ausencia parcial o total de un cromosoma X que conlleva una disgenesia gonadal y un fenotipo característico, entre los que destaca la talla baja. OBJETIVOS: Análisis de parámetros clínicos y auxológicos así como las características del seguimiento, tratamiento con GH y la respuesta a éste. MATERIAL Y MÉTODOS: Estudio observacional retrospectivo de 24 pacientes con diagnóstico genético de ST y que en 2011 presentaran una edad ósea >15 años. Fueron excluidas del estudio todas las pacientes que estuvieran recibiendo en la actualidad tratamiento con GH, así como aquellas que realizaron menos de 6 meses de tratamiento. RESULTADOS: El 100% de las pacientes revisadas presentó talla baja así como hipogonadismo hipergonadotropo, seguido de paladar ojival (83%), alteraciones torácicas y del cuello (75%), deformidad auricular (58%), cúbito valgo (58%) y otitis de repetición (50%). Otros hallazgos característicos de este síndrome como ptosis palpebral, linfedema neonatal, nevus pigmentados o alteraciones cardiovasculares se presentaron entre un 30-40%. Se registró una monosomía completa en el 42% de los pacientes, siendo el resto mosaicismos; de los que el más frecuente fue el 45X /46XX (33%), seguido de 45X /46Xi (Xq). No se apreció correlación entre fenotipo y genotipo. Se detectó una talla al inicio del tratamiento de 121’3+14’1 cm, con una talla proyectada de 145’3+4 (-1’96DS). Se administró tratamiento con GH recombinante durante una media de 7’2 años, a una dosis en el primer año de 0.042+0’005 mg/kg/dia. La edad media de estrogenización fue de 13’07 años. Se obtuvo una talla adulta de 151’07+2’7cm (-1’23DS), con un incremento con respecto a talla proyectada de 5’75+3 cm (+0’73DS). CONCLUSIONES: En nuestro estudio se ha observado que el ST tiene una expresividad fenotípica muy variable no correlacionada con el cariotipo, siendo el hallazgo más frecuente la talla baja. Dependiendo de la dosis usada, tiempo de tratamiento y edad de estrogenización, la terapia con GH puede conseguir una talla final > 150 cm., lo cual coincide con la literatura revisada.
P1d2d3-141 GEN FGFR3: UNA MUTACIÓN POCO FRECUENTE M.M. Hawkins Solís, A. Alcalde de Alvaré, J. Yebra Yebra, V. Quintero Calcaño, M. J. Trujillo-Tiebas, A. Cañete Díaz Hospital Infanta Sofía, Madrid INTRODUCCIÓN Presentamos el caso de un niño con sospecha de displasia ósea, en el que se ha descrito una nueva mutación en el gen del FGFR3. La misma mutación ha sido descrita en la madre, que muestra talla baja disarmónica. CASO CLÍNICO Paciente de 5 meses remitido a la consulta por talla baja a expensas de acortamiento de miembros. Antecedentes Personales: Embarazo controlado. EG: 37 + 4 semanas. Parto instrumental. Rea II. Apgar 8/9. Peso: 2625 gr (p16, -1DE). Longitud: 49 cm (p49, -0,04DE). Hiperbilirrubinemia neonatal que precisó fototerapia intensiva. Antecedentes Familiares: Talla padre 163 cm (p2, -2.23DS). Talla madre 147 cm (p<1, -2.85DS). Tallas familiares bajas en rama materna. Talla diana 161.5 ± 5 cm (p<1, -2.47DS) Exploración física a los 5 meses de edad: Peso: 7.1 kg (p18, -0.92 DE). Talla: 62 cm (p2, -2.13 DE). Perímetro Cefálico: 42.5 cm (p12, -1.2 DE). Impresiona de acortamiento de miembros a expensas de segmentos proximales. Fenotipo normal, no rasgos dismórficos llamativos salvo discreto abombamiento frontal. Exploración por aparatos normal. Exploraciones Complementarias: Hemograma y bioquímica normales. Inmunoglobulinas, estudio celiaquía, función tiroidea y Alfa 1 antitripsina: normales. IGF-I e IGF-BP3: normales. Rx muñeca izda: edad ósea acorde. Ecografía transfontanelar: normal. Cariotipo: 46 XY normal. Estudio gen SHOX: normal. Serie ósea: estructuras óseas de morfología normal. Acortamiento de segmentos proximales de miembros superiores e inferiores. Estudio molecular del gen FGFR3 (realizado mediante PCR + secuenciación del exón 8 del gen FGFR3): no se ha encontrado la mutación más común responsable de la acondroplasia, la transición G->A en la posición 1138. Se detecta el cambio c.1150T >C en heterocigosis respecto a la secuencia normal. Se realiza estudio a los padres y se detecta que la madre es portadora de la mutación identificada en el caso índice (c.1150T >C en heterocigosis). CONCLUSIONES Describimos una mutación del gen FGFR3 poco frecuente en la literatura. Esta mutación genera un cambio en la secuencia de aminoácidos (p.Phe384Leu) que ha sido previamente descrito en 2 familias con Displasia Esquelética mostrando una expresividad variable, desde una clínica suave a una más severa.
P1d2d3-142 SÍNDROME DE PRADER WILLI EN TRATAMIENTO CON GH L. Salamanca Fresno (1), N. Marín Huarte (1), C. Zozaya Nieto (1), L. Fernández (2), R. Gracia Bouthelier (1), I. González Casado (1) (1) Servicio de Endocrinología Pediátrica, Hospital Universitario La Paz, Madrid; (2) Instituto de Genética Médica y Molecular (INGEMM) Introducción: El síndrome de Prader-Willi (SPW) se caracteriza endocrinológicamente por obesidad, talla baja e hipogonadismo. El tratamiento con hormona de crecimiento (GH) permite una mejoría del crecimiento, composición corporal y capacidad física. Objetivo: valorar el tratamiento con GH en una serie de pacientes con SPW desde la aprobación de su uso en esta patología. Material y métodos: Se recogen 8 pacientes (6 varones y 2 mujeres) con SPW confirmado genéticamente y sospechado por criterios de Holl. El 63 % presentaban deleción paterna en 15q11-q13 y el 37 % disomía uniparental materna. Se administró GH en los 8 pacientes con dosis media inicio de 0,98 mg/m2/día durante un período medio de 6,39 años. Un modelo de regresión de “efectos mixtos” fue el elegido para establecer las comparaciones. Resultados: Se recogen entre otros los siguientes datos (tabla 1) antes de iniciar GH y en la última revisión con tratamiento. En 2 pacientes fue retirado el tratamiento por ineficacia a una edad media de 15,1 años; los datos se recogen en la tabla 2. Se comparó antes y después del tratamiento a los pacientes con deleción paterna frente a los pacientes con disomía uniparental materna obteniendo en los primeros, mayor mejoría en desviaciones estándar de talla, IMC y en el % de masa grasa (de manera significativa). Discusión: A pesar de que los datos presentan una amplia dispersión, la GH supone una mejoría sobre el crecimiento y la composición corporal en los pacientes con SPW, de manera global pero sobre todo en los debidos a deleción paterna.
P1d2d3-143 PREVENCIÓN DURANTE LA INFANCIA DE LA OSTEOPOROSIS DEL ADULTO. VALORES NORMALES DE CALCIFICACIÓN ESQUELÉTICA DESDE LOS 3 HASTA LOS 30 AÑOS, CON ESPECIAL REFERENCIA A LOS ESTADÍOS PUBERALES C. Rueda Caballero (1), M. Ruiz-Echarri Zalaya (2), N. García Sánchez (3), A. de Arriba Muñoz (1), (4), J.I. Labarta Aizpún (5), E. Mayayo Dehesa (5), A. Ferrández (1) Centro “Andrea Prader”, DGA, Zaragoza. (2) Hospital General Defensa, Zaragoza. (3) C.A.P. “Delicias Sur”, Zaragoza. (4) Hospital “Obispo Polanco”, Teruel. (5) Hospital Infantil Universitario “Miguel Servet”, Zaragoza. INTRODUCCIÓN. La adecuada osificación infantil y puberal es importante para atenuar la osteoporosis del adulto. OBJETIVO. Establecer valores normales de calcificación ósea por ultrasonidos de 3 a 30 años, adecuados al desarrollo puberal. CASUÍSTICA. 586 casos normales: 312 entre 3 y 8/10 años: 148 niñas, 164 niños; 189 (106 mujeres y 83 hombres) según estadío puberal y 85 adultos (44 mujeres y 41 hombres) entre 26 y 30 años. MATERIAL Y MÉTODOS. Densitómetro Bone Profiler DBM Sonic (IGEA) manejado por la misma médico que en estudios previos. RESULTADOS. Mujeres. Edades medias, en años, de cada estadío puberal: B1 (último control pre-puberal) : 9.9; B2: 10.8; B3: 11.7; B4: 15.5; B5: 17.8. Edad media adulta: 27.3 años. Se observan los siguientes aumentos de velocidad de ultrasonidos en m/seg.: 1) de 3 años a B1: 63.4, (3.37%); 2) de B1 a B5: 175.2, (9.13%), (68% de la ganancia total), observándose el incremento máximo de B3 a B4, de 90.3, (4.56%), (51.5 % del total puberal); 3) de B5 a edad adulta, sólo 19.4, (0.92 %). Varones. Cinco grupos según el volumen testicular (VT) y sus edades medias: 1) VT ≤3 ml (último control pre - puberal): 11.2 años; 2) VT > 4 < 8 ml: 12.8 años; 3) VT >9 < 13 ml: 15.9 años; 4) VT > 14 < 18 ml: 17.6 años; 5) VT > 19 < 25 ml: 17.9 años. Edad media adulta: 27.9 años. Se observan los siguientes aumentos de velocidad de ultrasonidos en m/seg. : 1) de 3 años a VT≤3: 85.5 ( 4.61%); 2) de VT ≤3 a VT > 19 < 25 ml: 188.1, (9.76%), (62% de la ganancia total), observándose el incremento máximo de VT 9-13 a VT 14-18 ml, de 85.5, (4.28%), (45.4% del total puberal); 3) de 17.9 años a la edad adulta, sólo 31.8 (1.5%). CONCLUSIONES. Nuestro estudio de la masa ósea de los 3 a los 30 años, muestra un incremento máximo durante el estadío puberal previo al adulto, en ambos sexos y una desaceleración desde éste al final de la tercera década. (Contribución especial para este estudio de la Obra Social de Ibercaja Zaragoza).
P1d2d3-144 COMPARACIÓN DE LA HISTOLOGÍA Y EXPRESIÓN DE SHOX EN LA PLACA DE CRECIMIENTO HUMANA EN UN FETO CON DML, HOMOCIGOTO PARA LA MUTACIÓN p.A170P V. Barca Tierno (1), S. Benito Sanz (1), E. Barroso (1), T. Vendrell (2), K.E. Heath (1) (1) Instituto de Genética Médica y Molecular, Hospital Universitario La Paz, Madrid, y CIBERER, ISCIII; (2) Depto de Genética, Hospital Universitario Vall d’Hebron, Barcelona INTRODUCCIÓN: El gen SHOX está localizado en la región pseudoautosómica 1 (PAR1) de los cromosomas sexuales. Mutaciones en dicho gen, están asociadas a pacientes con discondrosteosis de Léri-Weill (DLW) y displasia mesomélica de Langer (DML). Recientemente, hemos detectado la presencia de una mutación, c.508G>C (p.A170P) en 12 familias gitanas con DLW/DML, procedente de un ancestro común. El aminoácido Ala170 está localizado en la señal de localización al núcleo de la proteína SHOX. Esta mutación, inhibe el transporte de dicha proteína al núcleo. OBJETIVOS: Comparar la histología y expresión de SHOX en la placa de crecimiento humana en un feto de 22 semanas con DML, homocigoto para la mutación p.A170P frente a un feto normal de las mismas semanas de gestación. MÉTODOS: Examen físico y análisis histológico del feto con DML. Comparar la expresión de SHOX, mediante inmunohistoquímica, en la placa de crecimiento humana en ambos fetos. RESULTADOS: Las medidas del feto con DML comparado con los rangos de normalidad son: cubito (9 v 24-37mm), radio (19 v 24-34 mm), húmero (30 v 32-45mm), tibia (25 v 25-39mm), peroné (11 v 21-37mm) y fémur (32 v 29-44mm). Los análisis histológicos demuestran diferencias en ambos fetos. En el feto con DML se observa que los condrocitos en la zona de reserva son de mayor tamaño, con una forma redondeada y con tendencia a agruparse en parejas. En la zona proliferativa, las columnas aparecen menos definidas formando pequeños grupos. La expresión de SHOX mutante ha sido observada en todos los condrocitos de las zonas de reserva, proliferativa e hipertrófica al igual que en el feto normal. CONCLUSIONES: El acortamiento mesomélico y rizomélico de las extremidades de un feto con DML es muy evidente a las 22 semanas de gestación mediante ecografía. Se ha investigado por primera vez, el efecto de la expresión de SHOX en la placa de crecimiento humana en un feto con DML. Recomendamos el análisis de la mutación p. A170P de SHOX como primer paso para detectar el defecto molecular en pacientes con DLW y DML de raza gitana. Ofrecemos estudios prenatales cuando hay riesgo de afectación con DML.
P1d2d3-145 PRECISIÓN Y FIABILIDAD DE LA MEDICIÓN DE TALLA EN LA CONSULTA DE ENDOCRINOLOGÍA (1) D. López de Lara, (1) O. Pérez Rodríguez, (2) E. Gómez Hoyos (1) Servicio Pediatría; (2) Servicio Endocrinología, Hospital Clínico San Carlos, Madrid Introducción: Los dos principales componentes de la fiabilidad de la medición de talla son la Precisión y la Reproductibilidad de dicha medición de talla. El análisis y expresión del control de calidad de datos, frecuentemente presente en los estudios de laboratorio, se encuentra habitualmente ausente en los estudios antropométricos relacionados con el crecimiento. Objetivos: 1.- Estudiar la fiabilidad y precisión de la medición de talla en nuestra consulta de Endocrinología. 2.- Comparar la primera medida con la media de las otras dos. 3.- Evaluar el impacto de la precisión de la medida sobre la velocidad de crecimiento. Material y métodos: Dos observadores, un adjunto de Endocrinología pediátrica (AEP) y un Residente de 4º año de Endocrinología (R4E), realizaron 3 mediciones sucesivas ciegas en 113 pacientes de ambos sexos (42 niños/71 niñas) con edades comprendidas entre 2 y 18 años y tallas entre 78-181 cm. Las mediciones fueron realizadas con un estadiómetro Harpenden analógico (Holtain Ltd) con una precisión de 0,1 cm. Resultados: El AEP presentó una mediana de desviación estándar de la medición (DEmed) de 0,15 (RIC: 0,09-0,25) lo cual supondría un IC95% sobre la medición (Medida ± 2 x 0,15). La DEmed mediana del R4E fue 0,19 (RIC: 0,10-0,25) y el correspondiente IC95% de la medición (Medida ± 2 x 0,19). No se observó diferencia estadísticamente significativa entre la DEmed del R4E y la del ADP (p=0.152). El coeficiente de correlación intraclase de la primera medida vs la media de las otras dos, tanto para el ADP como para el R4E, resulto CCI>0.99 [IC95%: >0.99; >0.99]. Al comparar la primera medida del R4E vs la del ADP se obtuvo un CCI>0. 99 [IC95%: >0.99; >0.99]. Conclusiones: 1.- Ambos observadores presentan una alta precisión (Mediana de la DEmed de la medición <0,25) y reproductibilidad (CCI > 0.99) en sus mediciones. 2.- Realizar la media de dos mediciones sucesivas no difiere de realizar una única medición. 3.- La imprecisión de la medición de la talla puede hacer variar de forma preocupante el percentil de la velocidad de crecimiento (datos no mostrados) incluso cuando las medidas son realizadas por observadores demostradamente precisos. |
| References |